| 独立行政法人 理化学研究所 神戸研究所 発生・再生科学総合研究センター |
| 2008年6月5日 |
非常に長い臓器である腸管は、腸管壁にある神経ネットワークによって制御を受けてぜん動し、消化された内容物を体外へと送り出す。腸管の神経制御が失われると内容物が腸管内に蓄積し重度の便秘や腸閉塞をおこす原因となり得る。ヒルシュスプルング病と呼ばれる疾患はこの消化管の動きを制御する神経ネットワークが先天的に直腸や下部大腸で欠如し、腸管が正常に運動せずに内容物が移動できなくなり、腸の肥大をおこす病気である。 今回理研CDBの上坂敏弘研究員(神経分化・再生研究チーム、榎本秀樹チームリーダー)らは、マウスにおいてヒルシュスプルング病の主な原因遺伝子であるRet遺伝子の発現を低下させることによってヒルシュスプリング病様の腸管神経系の形成不全がみられることを明らかにした。このマウスはヒルシュスプルング病モデルマウスとして病気のメカニズム解析や治療法開発に非常に有効であると期待される。この研究成果はThe Journal of Clinical Investigation誌の5月号に掲載された。
上坂研究員らは、先行研究において神経栄養因子GDNF (Glial cell line-derived neurotrophic factor)の結合受容体であるGFRα1をマウス胎生後期のみ時期特異的に不活化すると、大腸下部における腸神経節がほぼ完全に消失することを見いだした。上坂研究員によると今回のモデルマウスを作ったきっかけは下記のとおりである。
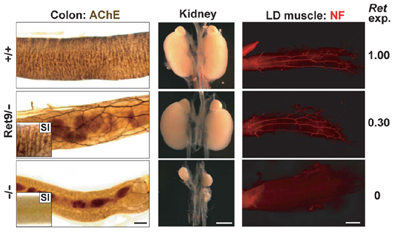
GDNF、GFRα1もしくはRetを完全に欠損したマウスでは、胃以降の腸管壁内神経節が形成されない。これは腸神経がないという意味ではヒルシュスプルング病に類似した表現型といえるが、実際にはこのような劇的なタイプはごくまれで、多くの患者では大腸下部にのみ神経欠損がおこる。またこれまでに報告されているRetの変異マウスは、腎臓や運動ニューロンにも発生異常が出る点でヒルシュスプルング病の病態と異なっている。発症メカニズムの解析にはより適切なモデルマウスが必要である。 「まず条件的にRetを欠損するマウスを作製し、胎児期後期にRetを不活化するとGFRα1の時と同様に大腸下部において神経系がなくなることを確認した。近年、ヒトのヒルシュスプルング病とRetの遺伝子発現を制御する領域の変異が関係していることが報告され、Ret遺伝子の発現量の低下が発症に寄与していることが示唆された。そこでRetの遺伝子発現レベルを抑えたマウスを作製して解析を行った。」 Ret発現量が50%に落ちるヘテロマウスでは症状が現れない。しかし上坂研究員がRet遺伝子の発現量が約30%に抑制されているマウスを作製して解析したところ、大腸下部において腸管壁内神経節が欠如したマウスが生まれてくることがわかった。このマウスでは腎臓の発生、運動ニューロンの投射に異常は見られなかった。またメスよりオスでより多く発症している傾向が見られ、この点もヒルスシュプルング病と類似していた。 次に上坂研究員らはこのモデルマウスを用いてRet遺伝子発現レベルの減少がどのようにして腸管壁内神経節の形成不全を引き起こすのか更なる解析を行った。Ret低発現マウス胎児では、腸神経堤細胞の腸管後部への移動に遅延がみとめられた。また胎生後期にRet遺伝子発現を低下させると大腸下部の神経節が消失した。このことから、Retの発現レベルの低下は腸神経細胞の生存、維持に支障をきたし、そして生じる神経細胞死がヒルシュスプルング病の発症に関与することが示唆された。
上坂研究員は「これまでRet遺伝子変異を原因とするヒルシュスプルング病は神経細胞死によるものではなく、腸神経堤細胞の移行がおかしくなって生じると考えられてきた。今回、モデルマウスの作製により生存シグナルの低下による神経細胞死の関与を示す結果が得られた。さらに解析を進めることで発症メカニズムの生物学的理解を深めることに貢献したい」と語る。今後このマウスを利用してヒルシュスプルング病の病理解明や新たな治療法開発といった医学的応用が期待される。
|
|||||
|
|||||
 |
| Copyright (C) CENTER FOR DEVELOPMENTAL BIOLOGY All rights reserved. |