| 独立行政法人 理化学研究所 神戸研究所 発生・再生科学総合研究センター |
2011年4月7日 |
胚発生が進み大まかな体のプランができあがると、眼や腎臓といった様々な器官の形成が始まる。これらの器官は、多数の種類の細胞を含む複雑な立体構造をもち、細胞間の連鎖的な相互作用の結果として生み出されると考えられている。そのため、器官や臓器の複雑な構造は、組織同士が精密に組み合う胚発生のなかでこそ形成可能、というのが一般的な考え方だ。しかし、本当に器官の原基や小さな臓器を試験管の中でつくり出すことはできないのだろうか。 理研CDBの永樂元次副ユニットリーダー(立体組織形成・解析ユニット)と笹井芳樹グループディレクター(器官発生研究グループ)らは、この課題に「自己組織化」というアプローチで挑んだ。自己組織化とは、細胞の集団が自律的に複雑な構造を生み出す機序をいう。今回、彼らはマウスES細胞から自己組織化を誘導することで、網膜の原基である「眼杯」を試験管内で立体構築することに成功し、それを可能とする組織内の細胞動態メカニズムを明らかにした。さらに、この眼杯を長期培養し、生後の眼と同様の多層構造をもつ神経網膜の形成にも成功した。この研究は、理研VCADプログラム、京都大学、大阪大学との共同で行われ、4月7日発行のNature誌に発表された。
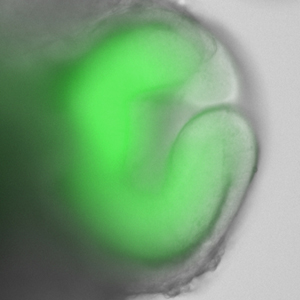
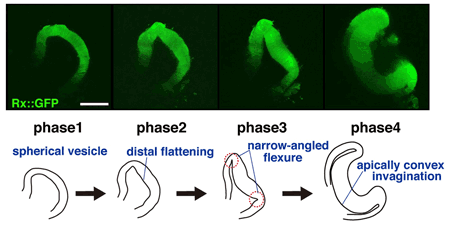
眼杯の発生は古くから発生生物学の重要なテーマであったが、その形成メカニズムについては2つの説が対立してきた。網膜は間脳に由来する中枢神経組織で、その発生は、初期胚で間脳の側方が袋状の上皮構造として突出し、眼胞と呼ばれる構造を形成することから始まる。次に、眼胞の上皮組織は、その遠位の先端部が袋の中へ陥没してカップ状の眼杯となる。そのため、眼杯は上皮組織の2重壁構造をもち、成熟すると外側が色素上皮、内側が神経網膜になり、網膜の原基が完成する。眼杯の形成と同時に、表皮外胚葉からは水晶体や角膜が誘導され、それらが組み合わさって眼球が完成する。実験発生学の父、ハンス・シュペーマンは、眼杯の形成には水晶体や角膜の組織は不要である可能性を示していたが、その後の多くの実験は、これらの組織が眼胞の陥没に必要であることを主張していた。 同研究グループではこれまでに、神経発生学の知見に基づき、ES細胞から各種神経細胞を誘導することに成功してきた。近年、中枢神経系の誘導に適した無血清浮遊培養法「SFEBq法」を開発し、層構造をもった大脳皮質様組織を試験管内で構築することにも成功していた。今回彼らは、SFEBq法の培地組成を変更した上、細胞外マトリクスタンパク質を添加するなどして、網膜組織の誘導に適した培養条件を見出した。この方法でES細胞の細胞塊を培養すると、明確な上皮構造をもつ網膜前駆組織が高効率に誘導され、分化培養開始7日後にはその一部が袋状に突出した。さらに培養開始後9日後にはこの眼胞様組織の先端が陥没し、10日後までに2層構造からなる眼杯様組織が形成された。内側の層では神経網膜、外側の層では色素上皮に特徴的な遺伝子発現が認められ、誘導された組織が眼杯と同等であることが確認された。一方で、この眼杯の周囲に他の組織は無いことから、眼杯は水晶体などの組織が無くても自己組織化によって自律的に形成され得るこが示された。 次に彼らは、この自己組織化のメカニズムを探るために、多光子励起蛍光イメージング技術による3次元経時観察を行った。その結果、ES細胞由来の網膜前駆組織は、まず色素上皮と神経網膜の領域に自発的に分かれ、次に、胚の眼発生と同様に4ステップの組織変形を経て眼杯を形成することがわかった。この変形過程では、細胞骨格の調節による組織剛性の変化が起こり、陥没する領域ではミオシンの活性が低下し、上皮組織が変形しやすくなっていることも示された。また、陥没する領域では細胞分裂を駆動力とした上皮組織の拡張が必要であることが示唆された。
彼らは、眼杯形成を力学的観点からも詳細に検討するため、コンピューター解析による力学シミュレーションを行った。その結果、眼杯の形成は3つの力学的な局所ルールによって起こることが確かめられた。まず、眼胞の上皮組織の一部(将来の神経網膜)が柔軟性を獲得し、次に、陥没時の折り目となる部位(将来の神経網膜と色素上皮の境界)の細胞が三角錐状に変形し、そして、陥没部の上皮組織が細胞分裂によって面積を拡大する、というプロセスだった。これは、先に観察された細胞生物学的な機序と良く一致していた。 最後に、眼杯から神経網膜部分を切り出し、神経網膜の成熟を促す条件でさらに14日間3次元培養する実験を行った。その過程で、神経網膜の細胞は盛んに分裂し、生後の生体神経網膜と同様に6種類の主要細胞を含む多層構造を形成することがわかった。しかも、多層構造の順序は生体の神経網膜と同様で、シナプス形成も確認された。この結果は、神経網膜の複雑な全層構造も自律的に自己組織化し得ることを示していた。 今回の研究は、生体内では複雑で解析が難しい器官誘導のメカニズムを、ES細胞を用いた単純な培養系によって証明したことになる。笹井グループディレクターは、「眼杯形成や神経網膜の多層形成という複雑な組織形成が、実は網膜前駆細胞に内在するプログラムをもとに、自己組織化によって起こり得ることが明らかになりました。特に、眼杯の自己組織化については、シュペーマンの実験以来、1世紀に渡る論争に一つの結論を示すことができたと思います」と語る。一方で、「生体内では周囲の組織との間にも複雑な相互作用が存在し、それらが2重、3重に働いて、より精密な眼形成が再現性良く起きているのではないか」と推測する。今回の成果は医学への応用も強く期待される。「ES細胞やiPS細胞から、細胞ではなく組織のレベルで網膜を構築し、機能組織の移植によって網膜変性疾患を治療するという、新しい発想の再生医療の可能性が開けました」とコメントした。
|
|||||||||||||||
 |
| Copyright (C) CENTER FOR DEVELOPMENTAL BIOLOGY All rights reserved. |