| 独立行政法人 理化学研究所 神戸研究所 発生・再生科学総合研究センター |
| 2007年6月28日 |
動物の体は多種多様な細胞から構成されるが、なかでも特別な存在と言えるのが生殖細胞だ。生殖細胞、つまり精子と卵子は、受精によって次世代を構築できる唯一の細胞だ。このように一個体をつくり上げる能力を「全能性」と呼ぶ。生殖細胞の形成過程では、DNAやヒストンのメチル化状態がゲノムワイドに再編成され、これによって生殖細胞に特徴的な遺伝子発現が確立され、全能性の獲得が可能になると考えられている。しかし、メチル化状態がどのように変化し、生殖細胞がその本質的な機能を獲得するのかは未解明のままだった。 理研CDBの関由行基礎科学特別研究員(哺乳類生殖細胞研究チーム、斎藤通紀チームリーダー)らはマウスをモデルにした研究で、始原生殖細胞(PGCs; primordial germ cells)が、ヒストンのメチル化状態を変化させながら成熟していく様子を詳細に明らかにした。始原生殖細胞が生殖腺へと移動する過程で、メチル化の再編成が徐々に起きていることがわかった。この研究は、国内の複数の研究機関と共同で行われ、Development誌に6月13日付でオンライン先行発表された。
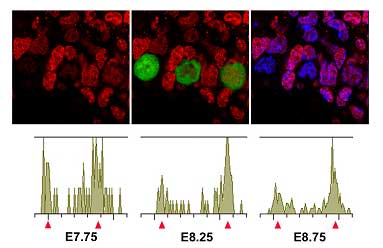
彼らは以前の研究で、発生6.25日目に胚盤葉上層の少数の細胞がBlimp1と呼ばれる遺伝子を発現し、これらの細胞がstellaを発現する始原生殖細胞に分化することを明らかにしていた。始原生殖細胞は発生7.5日目頃から生殖腺へと移動を始め、生殖細胞としての運命を確実にしていく。また彼らは、始原生殖細胞が生殖腺へと移動する過程で、DNAのメチル化およびヒストンH3の9番リジンにおけるジ(di-)メチル化(H3K9me2)がゲノムワイドに減少し、それと対照的にヒストンH3の27番リジンにおけるトリ(tri-)メチル化(H3K27me3)が高レベルに起きることを報告していた。 関研究員らは今回、生殖細胞の発生に伴うヒストンメチル化の動態を詳細に追った。まず、Blimp1を発現する始原生殖細胞前駆体と周囲の体細胞とを比較したところ、この時点ではメチル化状態に有意な差は見られなかった。解析を進めると、H3K9のジメチル化レベルは発生7.75日目頃から低下し始め、8.75日目には非常に低いレベルにまで落ちていることがわかった。これはちょうど、始原生殖細胞が生殖腺へと移動して行く時期と重なっていた。また、H3K9のジメチル化レベルの低下は、脱メチル化酵素の特異的な活性化によるものではなく、メチル基転移酵素の抑制により開始されることが示唆された。これとは逆に、H3K27のトリメチル化レベルは発生8.25日目頃から上昇し、9.5日目には約85%の始原生殖細胞が強いトリメチル化シグナルを示した。 続いて彼らは、始原生殖細胞の細胞周期とメチル化再編成との関係について調べた。すると、始原生殖細胞はH3K9の脱メチル化の開始に先立ってG2期停止を起こし、H3K27のトリメチル化が完了する頃に細胞周期を再開することがわかった。このことから、ゲノムワイドなメチル化の再編成は、始原生殖細胞がG2期で停止している間に起きていることが強く示唆された。 H3K9のジメチル化は一般的に、その領域に含まれる遺伝子の発現を抑制することで知られる。そこで彼らは、始原生殖細胞における遺伝子発現の変化を調べることにした。全般的な発現活性の指標となるRNAポリメラーゼIIのリン酸化レベルを調べると、興味深いことに、H3K9の脱メチル化の開始後からH3K27のトリメチル化が完了する時期にかけて、リン酸化レベルが低下していることがわかった。このRNAポリメラーゼIIの活性低下は、ヒストンメチル化の再編成と関連して起きているようだったが、そのメカニズムは不明だった。 これらの結果から、生殖細胞形成におけるヒストンメチル化の大規模な再編成は、G2期停止した始原生殖細胞が生殖腺へと移動していく間に起きていることが明らかとなった。まず、H3K9のジメチル化レベルが低下し、次にRNAポリメラーゼIIの活性が低下、続いてH3K27のトリメチル化レベルが上昇し、RNAポリメラーゼIIの活性が復活するといった順序だ。斎藤チームリーダーは、「哺乳類の生殖細胞形成は、エピジェネティックな情報のゲノムワイドな再編成を生体内で解析できる最良のモデルだろう。生殖細胞による全能性獲得のメカニズム解明は、体細胞リプログラミングの分子機構にも大きなヒントを与えると考えられる」と話す。 |
|||||
|
|||||
[ お問合せ:独立行政法人 理化学研究所 神戸研究所 発生・再生科学総合研究センター 広報国際化室 ] |
| Copyright (C) CENTER FOR DEVELOPMENTAL BIOLOGY All rights reserved. |