| 独立行政法人 理化学研究所 神戸研究所 発生・再生科学総合研究センター |
| 2007年10月26日 |
体内時計はバクテリアからヒトまで多くの生物種に保存された生体システムで、ヒトでは睡眠や覚醒、ホルモン分泌を始めとする様々な生理機能を調節している。体内時計の実体は、時間周期的な遺伝子発現を繰り返す時計細胞であり、哺乳類の場合、視交叉上核を中心に体の様々な部位に散在している。これらの細胞が刻む約24時間周期のリズムが同調することによって、個体全体としてのリズムが作り出されている。
1970年、真夜中に強い光を浴びると体内時計が一時的に停止してしまう現象がショウジョウバエで発見された。後に哺乳類を含む多くの生物でも同じ現象が確認され、「シンギュラリティ現象」と呼ばれるようになった。しかし、体内時計の停止が個々の時計細胞のリズム停止によるものなのか、時計細胞同士の脱同調によるものなのかは、謎のままだった。
理研CDBの鵜飼英樹研究員、小林徹也研究員(システムバイオロジー研究チーム、上田泰己チームリーダー)らは、光受容体を導入した光応答性時計細胞を創出して解析を行い、真夜中の強い光で体内時計が一時的に停止するのは、個々の時計細胞のリズムが脱同調した結果であることを明らかにした。この成果は、近畿大学、名古屋大学との共同研究によるもので、英国の科学誌Nature Cell Biologyに10月21日付けでオンライン先行発表された(11月号誌面に掲載予定)。
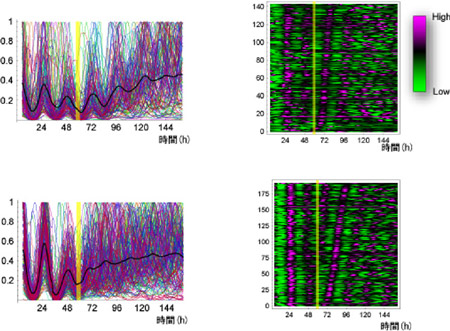
「もし試験管の中で体内時計を一時的に停止させることができれば、個々の時計細胞の状態を詳細に解析し、シンギュラリティ現象の難問を解決できるのではないか」と彼らは考えた。そこでまず、本来光を感じることができない哺乳類時計細胞に、メラノプシンと呼ばれる光受容体タンパク質を導入し、光応答性時計細胞をつくりだした。メラノプシンは光刺激により、体内時計に影響を与える細胞内カルシウムの濃度を変化させる。彼らは、この細胞集団に様々なタイミングと長さで光刺激を与え、体内時計のリズムがどのように変化するのかを調べた。この実験を繰り返した結果、光刺激によって体内時計の位相や振幅を自在に操り、さらには試験管の中で体内時計を一時的に停止させる、つまりシンギュラリティ現象を再現することに成功した。 次に彼らは、細胞集団としては停止したように見える時計細胞の概日リズムを1細胞レベルで測定した。すると、シンギュラリティ現象が生じるタイミング(細胞にとっての真夜中;主観的真夜中)で光を照射すると、1細胞単位での概日リズムは維持されているものの、細胞同士の位相のばらつきが急激に増幅し、完全に脱同調してしまうことが明らかとなった(図)。彼らは、シンギュラリティ現象を生じるタイミングがなぜ主観的真夜中なのかについても、数理モデルを用いて理論的に立証している。
上の実験により、培養した時計細胞における概日リズムの消失は、個々の細胞のリズム消失ではなく、脱同調に起因していることが示された。しかし、同じことが生体内でもおきているのだろうか。彼らはこの疑問に答えるために、ラットに主観的真夜中付近で光を照射し、視交叉上核における時計細胞の遺伝子発現を解析した。すると光刺激後には、視交叉上核全体で見ると時計遺伝子の発現周期が乱れていたが、各部位を詳細に観察すると、それぞれの部位では明確なリズムが維持されていた。また、光刺激を与えたラットでは、昼夜の行動量の差が小さくなることも確認された。これにより、生体内においても、真夜中の光照射によって時計リズムの脱同調が起きていることがわかった。
今回の研究は、30年以上謎のままだったシンギュラリティ現象のメカニズムだけでなく、体内時計の光刺激による脱同調・同調のメカニズムも明らかにしている。数理学的に詳細な解析を行った小林は、「時計細胞は互いに同調しながらも、一定の範囲で揺らぎをもってリズムを刻んでいます。これにより、体内時計システムは外的環境の大きな変化に適応しつつ、多少の変化には惑わされずに一定のリズムを刻む、非常にバランスの取れたシステムと言えます」と話す。また、彼らはこの研究はシステムバイオロジーの概念が鍵になっているという。定量的な光制御を実現した鵜飼は、「1細胞レベルでの詳細なモニタリング系、ハイスループットな測定系、実験データに基づく数理モデルの構築を基盤とし、時空間的・定量的に厳密な制御が可能な光刺激を用いることで、試験管内および生体内における時計細胞のリズム解析が可能になりました」と話す。 |
||||||
|
||||||
| [ お問合せ:独立行政法人 理化学研究所 神戸研究所 発生・再生科学総合研究センター 広報国際化室 ] |
| Copyright (C) CENTER FOR DEVELOPMENTAL BIOLOGY All rights reserved. |